靶向离子通道的骨关节炎治疗药物简介
一、骨关节炎简介
骨关节炎(osteoarthritis,OA)是最常见的关节炎形式,约占全球人口的7%,全球人口超过5亿人,其中50岁以上人群和女性受累尤为严重,OA最常见的症状是疼痛、僵硬、肿胀、畸形和关节功能下降。现有临床治疗主要涉及药物、非药物和手术方式。然而,目前既没有有效的OA治疗方法,也没有早期诊断或评估药物疗效的方法。

二、软骨细胞表面离子通道
软骨细胞是关节软骨中的主要常驻细胞,是软骨组织的主要结构者,主要负责所有细胞外基质(ECM)大分子的合成和维持。软骨细胞的独特之处在于它们能够在低氧张力微环境中生存,并且大多数能量需求是通过糖酵解而不是氧化磷酸化获得的。所有活细胞都具有电学特性并具有膜电位。一般来说,只有肌肉和神经细胞被认为是“可兴奋的”,而软骨细胞由于细胞质隔离,因此是“不可兴奋的”。尽管是不可兴奋的细胞,但软骨细胞表面包含如钠-钾ATP酶、电压依赖性钙通道(VDCC)、配体门控Ca2+进入途径-嘌呤能受体、N-甲基-D-天冬氨酸受体、瞬时受体电位(TRP)通道等多种离子通道如图1所示。
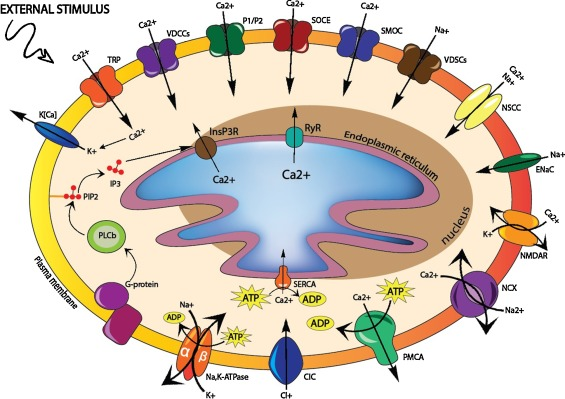
软骨细胞涉及离子通道示意图[1]
(源引:Joint Bone Spine.2019)
三、病理情况下软骨细胞表面离子通道的改变
骨性关节炎现在被认为远比单纯的“磨损”疾病更具炎症性,在人软骨中检测到5种不同电压门控钠通道(VGSC)的表达,包括Nav1.1β、Nav1.2β、Nav1.2α、Nav1.3α和Nav1.6α和Nav1.7,VGSCs被证明参与维持兔关节软骨细胞的膜电位。最新研究通过对正常和OA组进行RNA测序(RNA-seq)分析[2],结果显示Nav1.7是显著上调、与OA相关电压门控通道,该通道特异性阻断可显著调节细胞内Ca2+信号传导和软骨细胞分泌组份,改善结构性关节损伤的进行性发展,并减少OA疼痛行为。揭示Nav1.7可作为保护软骨细胞和止痛治疗的双重靶点进行药物开发。
四、离子通道调节剂对OA的影响
目前研究认为骨关节炎(OA)和心血管疾病(CVD)具有许多相似的特征,包括相似的危险因素和分子机制。大量的心血管药物通过不同的离子通道起作用,改变离子平衡,从而调节细胞代谢、渗透反应、软骨细胞外基质的更新和炎症[3]。研究表明,钙通道(尤其是L型Ca2+通道)拮抗剂(如维拉帕米和氨氯地平)可能通过减缓OA进展、增加ECM成分的产生、抑制软骨细胞肥大、上调软骨生成标志物糖胺聚糖、II型胶原、转录因子Sox9等使患者获益[4,5]。作为治疗心率失常的钠通道抑制剂利多卡因也广泛用于OA疼痛管理,但仅限于短期静脉使用,其对OA关节的长期影响尚不清楚。此外,在斑马鱼胚胎模型中,普鲁卡因胺的软骨元素和Sox9蛋白含量增加[6]。
五、MSC对OA软骨细胞中离子通道的影响
研究显示,TRPV4(瞬时受体电位香草素4)是一种机械传导钙通道,可调节软骨细胞对膝关节OA早期基质硬度改变的感知,TRPV4在OA进展过程中被激活,通过影响破骨细胞的分化参与疾病发展,MSC-Exos可通过影响TRPV4调节破骨细胞的活化,局部单次注射可有效改善异常的软骨下骨重塑,抑制了骨硬化和骨赘的发生,缓解了体内软骨退化和滑膜炎症[7]。考虑到MSC-Exos的治疗效果与局部微环境的调节密切相关,其改善软骨下骨重塑可能不仅源于对TRPV4介导的破骨细胞活化的直接抑制,还归因于免疫微环境,也受TRPV4本身的调控[8]。
综上所述,G细胞的应用为OA治疗提供了一种有前途的细胞疗法,但MSC对不同组织的潜在机制和疗效仍需进一步研究,尤其G细胞对其他类型电压依赖的离子通道是否有作用,通过阻断钠内流,而缓解疼痛,最终发挥标本兼治的功效。
参考文献:
1. Mobasheri A, Matta C, Uzielienè I, Budd E, Martín-Vasallo P, Bernotiene E. The chondrocyte channelome: A narrative review. Joint bone spine 2019, 86(1): 29-35.
2. Fu W, Vasylyev D, Bi Y, Zhang M, Sun G, Khleborodova A, et al. Na(v)1.7 as a chondrocyte regulator and therapeutic target for osteoarthritis. Nature 2024.
3. Vaiciuleviciute R, Bironaite D, Uzieliene I, Mobasheri A, Bernotiene E. Cardiovascular Drugs and Osteoarthritis: Effects of Targeting Ion Channels. Cells 2021, 10(10).
4. Mancilla EE, Galindo M, Fertilio B, Herrera M, Salas K, Gatica H, et al. L-type calcium channels in growth plate chondrocytes participate in endochondral ossification. J Cell Biochem 2007, 101(2): 389-398.
5. Takamatsu A, Ohkawara B, Ito M, Masuda A, Sakai T, Ishiguro N, et al. Verapamil protects against cartilage degradation in osteoarthritis by inhibiting Wnt/β-catenin signaling. PloS one 2014, 9(3): e92699.
6. Asad Z, Sachidanandan C. Chemical screens in a zebrafish model of CHARGE syndrome identifies small molecules that ameliorate disease-like phenotypes in embryo. European journal of medical genetics 2020, 63(2): 103661.
7. Fu Y, Cui S, Zhou Y, Qiu L. Dental Pulp Stem Cell-Derived Exosomes Alleviate Mice Knee Osteoarthritis by Inhibiting TRPV4-Mediated Osteoclast Activation. Int J Mol Sci 2023, 24(5).
8. Dutta B, Goswami R, Rahaman SO. TRPV4 Plays a Role in Matrix Stiffness-Induced Macrophage Polarization. Frontiers in immunology 2020, 11: 570195.